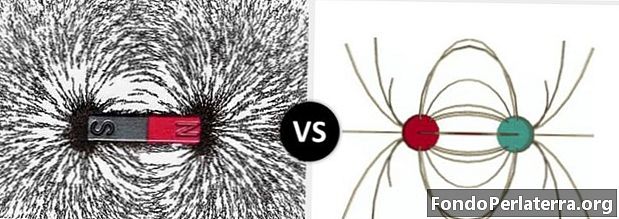
Kovalentās obligācijas salīdzinājumā ar jonu obligācijām
Saturs
- Saturs: atšķirība starp kovalentajām un joniskajām saitēm
- Salīdzināšanas tabula
- Kas ir kovalentās obligācijas?
- Kas ir jonu saites?
- Galvenās atšķirības
Galvenā atšķirība starp jonu saitēm un kovalentām saitēm ir elektronu pāru un atomu dalīšana. Kovalentās saitēs atomi ir elektrostatiski pievilkti viens pret otru, bet jonu saitēs; elektronu pāri tiek dalīti starp atomiem.
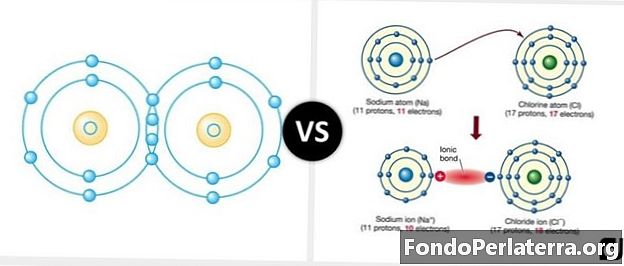
Saturs: atšķirība starp kovalentajām un joniskajām saitēm
- Salīdzināšanas tabula
- Kas ir kovalentās obligācijas?
- Kas ir jonu saites?
- Galvenās atšķirības
- Video skaidrojums
Salīdzināšanas tabula
| Atšķirības pamats | Kovalentās obligācijas | Jonu saites |
| Definīcija | Kovalentā saite ir ķīmiskās saites veids, kas ietver dalītu pāru vai saistošu pāru (elektronu pāri) sadalījumu starp atomiem. | Jonu saite ir ķīmiskās saites veids, kas ietver viena vai vairāku elektronu dalīšanos vai pilnīgu atdošanu no viena atoma uz otru atomu. |
| Notikums | Kovalentās saites ir neitrālu atomu mijiedarbības rezultāts | Jonu saites ir anjonu un katjonu mijiedarbības rezultāti. |
| Ķīmiskais potenciāls | Tās ir diezgan vājas ķīmiskās saites | Tie ir visspēcīgākais ķīmisko saišu tips. |
| Veidošanās | Nemetāliski elementi veido kovalentās saites | Metāliskie elementi veido jonu saites |
| Elektronu statuss | Kopīgi elektroni | Kopējā elektronu pārnešana |
| Jautājums par valsti | Šķidrumi un gāzes istabas temperatūrā | Cietvielas istabas temperatūrā |
| Savienojumi | Organisks | Neorganisks |
| Šķīdība | Nešķīst ūdenī | Šķīst ūdenī |
| Forma | Noteikta forma | Nav noteiktas formas |
| Nosaukšana | Grieķu valodas prefiksi | Romiešu cipari |
| Piemēri | Sālsskābe un metāns | Sērskābe un nātrija hlorīds |
Kas ir kovalentās obligācijas?
Kovalentās saites, ko sauc arī par molekulāro saišu nosaukumiem, ir ķīmisko saišu veids, kas ietver dalītu pāru dalīšanu vai saišu pāri (elektronu pāri) starp atomiem. Lielākajā daļā molekulu elektronu dalīšanās ļauj katram atomam iegūt pilnīga ārējā apvalka ekvivalentu, kas atbilst stabilai elektroniskai konfigurācijai. Ja atomiem ir līdzīga afinitāte pret elektroniem, visticamāk, notiks kovalentās saites, jo tā pati afinitāte pret elektroniem un nemēdz tos atdot. Atomi dalās ar elektroniem, lai iegūtu oktetu konfigurāciju un kļūtu stabilāki un stiprāki. Sigmas un pi orbitāļu mijiedarbības dēļ kovalentās saites var veidot četru veidu saites, proti, vienu, divkāršu, trīskāršu un četrkāršu. Skābekļa atomi ir labākais piemērs, kam nepieciešami divi papildu elektroni, lai izveidotu slēgtu apvalku, savukārt ūdeņraža atomiem ir vajadzīgs viens, lai izveidotu slēgtu apvalku. Skābekļa atoms dalās divos tā elektronos ar ūdeņraža atomiem, tāpēc abu atomiem ir slēgti apvalki. Tas galu galā rada ūdens molekulu.
Kas ir jonu saites?
Jonu saite ir ķīmiskās saites veids, kas ietver viena vai vairāku elektronu dalīšanos vai pilnīgu atdošanu no viena atoma uz otru atomu. Jonu saites ir to elementu rezultāts, kuri viegli zaudē elektronus, un to elementu rezultāts, kuri iegūst elektronus. Šāda veida saites molekulām vispār nav paredzētas lādiņu mijiedarbības dēļ, kā aprakstīts Kulona likumā. Jonu saites istabas temperatūrā saglabājas cietas, jo periodiski veidojoties režģiem ar miljardiem jonu, katru jonu ieskauj daudzi pretējas uzlādes joni. Elektrostatiskās atrakcijas starp negatīvajiem un pozitīvajiem joniem satur savienojumu kopā. Kopējā enerģija jonu savienošanas procesā parasti ir pozitīva, norādot, ka reakcija ir endotermiska un nelabvēlīga. No otras puses, šī reakcija vienlaikus ir labvēlīga to elektrostatiskās pievilcības dēļ. Biežs jonu saites piemērs ir nātrijs vai sāls. Nātrija atomi ātri dod elektronus, kas rada pozitīvu lādiņu. Hlors pieņem šos elektronus un ir negatīvi lādēts. Šie divi pretēji uzlādētie atomi pēc tam piesaista viens otru, veidojot nātrija hlorīda molekulu.
Galvenās atšķirības
- Kovalentās saitēs elektronu orbitāles pārklājas, bet jonu saišu gadījumā tās ir atsevišķas.
- Kovalentās saites ir salīdzinoši mīkstas, salīdzinot ar jonu saitēm, kas ir cietas un trauslas.
- Gan metālu atomi, gan nemetāla atomi ir iesaistīti jonu saišu veidošanā, bet kovalento saišu veidošanā; ir iesaistīti tikai nemetālu atomi.
- Kovalentās saites veidojas daloties elektroniem, savukārt jonu saites veidojas elektronu pārvietošanās dēļ.
- Molekulas ir daļiņas kovalentās saitēs savienojuma veidošanās laikā, savukārt jonu saitēs tie ir pozitīvi un negatīvi lādēti joni.
- Kovalentās saites nav vadītāji, bet jonu saites ir vadītāji.
- Kovalentais savienojums notiek starp atomiem, kuru elektronegativitāte maz atšķiras. Jonu saite notiek starp atomiem, kuriem ir lielas atšķirības elektronegativitātē.
- Jonu saitēm ir nepieciešama augsta kušanas temperatūra un viršanas temperatūra jonu saiti gadījumā. Kovalentajām saitēm ir nepieciešama zema kušanas un viršanas temperatūra kovalento saišu gadījumā.
- Metāns un sālsskābe ir parasti kovalenta nātrija hlorīda un sērskābes piemēri.
- Kovalentām saitēm ir noteikta forma, bet jonu saitēm nav noteiktas
- Kovalentām saitēm ir zema polaritāte, bet jonu saitēm ir augsta polaritāte.
- 100% kovalentās molekulas izšķīdīs eļļā, bet ne ūdenī, kamēr daudzām jonu saitēm ir iespēja izšķīst ūdenī, bet ne eļļā.
- Kovalentās saites ir svarīgas, jo oglekļa molekulas mijiedarbojas galvenokārt ar kovalento saišu palīdzību, savukārt jonu saites ir svarīgas, jo tās ļauj sintēt noteiktus organiskos savienojumus.
- Kovalentās saites var būt gan elementi, gan savienojumi, savukārt jonu saites var būt tikai savienojumi.